Linus Pauling fue un genio que modernizó la química en el siglo XX. Introdujo la aplicación de los métodos de la mecánica cuántica a la química, siendo uno de los fundadores de la química cuántica. A partir de estos estudios, se tuvo una imagen más clara de las estructuras atómicas y del enlace químico. Fue pionero en la aplicación de los métodos de determinación de estructuras químicas para caracterizar sustancias químicas (iónicos o moleculares) y relacionar esa información para explicar fenómenos químicos, incluyendo la función biológica, y relacionándola con la estructura. Fue el gran maestro de la química estructural. Pauling estaba convencido de que entender la estructura es la clave para descifrar algunos de los misterios del universo. Su interés en biología y su amplio conocimiento de la química estructural, le convirtió en uno de los funadadores de las nuevas disciplinas de la biología molecular y la biomedicina.

Pauling nació en Oregon el 28 de febrero de 1901. Quedó huérfano de padre siendo muy joven. Por problemas económicos familiares, se le recomendó que estudiase una carrera práctica que le permitiese encontrar trabajo pronto. Por eso eligió estudiar ingeniería química en la Oregon State University (OSU), graduándose en 1922.
Desde muy joven, pensaba que la física era fundamental para entender el comportamiento químico y decidió realizar la tesis doctoral en química física. Solicito realizar la tesis en el grupo de Arthur Noyes, en el Instituto Tecnológico de California (Caltech), uno de los químicos físicos más prestigiosos de la época. Parece ser que Noyes dudó en su contratación porque Pauling era un ingeniero químico que no había asistido a cursos de química física avanzada. Sin embargo, convenció a Noyes y éste le admitió en su grupo; donde terminó la tesis en 1925.
Becado por la Fundación Guggenheim (en la época en la que ser becario era un honor y no era una palabra denigrada como actualmente) realizó estancias postdoctorales entre 1926 y 1927. Reconociendo el papel que la ciencia europea estaba realizando para entender la estructura de la materia, trabajó en Copenhage con Niels Bohr (Premio Nobel de Física en 1922), en Münich con Arnold Sommerfeld (no recibió el Premio Nobel, pero lo mereció varias veces), en Londres con William H. Bragg (Premio Nobel de Física en 1915) y en Göttingen con Max Born (Premio Nobel de Física en 1954). Sin duda, recibió una excelente formación teórica y experimental en mecánica cuántica y en cristalografía; en definitiva, en las estructuras de sustancias químicas, ya sean átomos, sales o moléculas.
De vuelta a Estados Unidos, fue contratado como profesor en Caltech donde permaneció hasta su jubilación en 1973. Tras esta fecha y hasta su muerte, el 19 de agosto de 1994, Pauling trabajó como profesor emérito en la Stanford University, donde se creó el Linus Pauling Institute (LPI). Pauling investigó de manera continuada durante 72 años, siendo un testigo privilegiado y protagonista del mayor desarrollo de la historia de la química. Posteriormente, su legado fue trasladado desde el LPI a su Alma Mater, la OSU.
Pauling fue un excelente docente y divulgador de la ciencia. En esta última faceta era frecuente su participación en medios diversos explicando ciencia. Un ejemplo se puede encontrar en el vídeo http://www.youtube.com/watch?v=KDDQMTfMZxE.
En su faceta docente, parece que era un profesor espectacular al que le gustaba ilustrar sus explicaciones teóricas con demostraciones prácticas en clase. Hay una característica que le iguala con Mendeleev. Cuando éste tuvo que explicar Química general a sus alumnos de primer curso de la Universidad de San Petersburgo, no encontró ningún libro de texto que le satisficiera; por lo que decidió escribir su libro Principios de química, cuya redacción le inspiró para crear la tabla periódica. Lo mismo le pasó a Pauling. Cuando tuvo que explicar Química general a alumnos de primer curso de Caltech, se dio cuenta que lo mejor era escribir su propio libro de texto. Así nació su libro General Chemistry, cuya primera edición se publicó en 1947, constituyendo un clásico de la enseñanza de la química desde entonces.
Realizó aportaciones fundamentales en las bases teóricas de la química, usando la mecánica cuántica para explicar la estructura molecular y el enlace químico. Introdujo conceptos fundamentales como la resonancia y la hibridación. De estos estudios surgió el libro Introduction to Quantum Mechanics with Applications to Chemistry (escrito en colaboración con E. Bright Wilson) en 1935; un clásico en química cuántica.
Pauling propulsó la Teoría de Enlace de Valencia (TEV) como una teoría más química e intuitiva que la alternativa Teoría de Orbiltaes Moleculares (TOM) para explicar el enlace y la estructura molecular. Debido que la TOM es más fácilmente implantable en un programa computacional que la TEV, aquella se desarrolló más que esta.
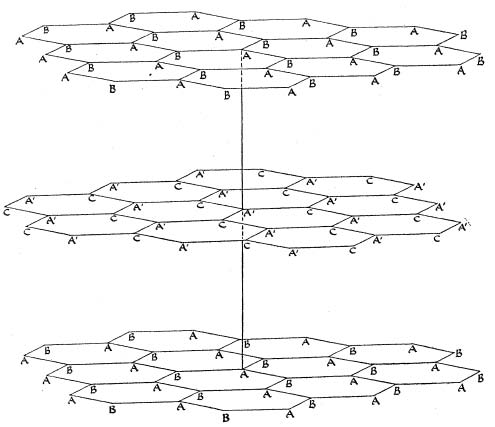
Pauling fue un pionero en el uso de la cristalografía en química, siendo el primer tema que desarrolló a su vuelta a Caltech en 1927. El uso de la difracción de rayos X y de la difracción de electrones le permitió profundizar en la estructura de compuestos inorgánicos (principalmente) y orgánicos y empezar a entender la naturaleza del enlace químico. De estas investigaciones surgieron las reglas de Pauling para predecir la estructura cristalina de compuestos iónicos y la escala de electronegatividad que desarrolló, que permitió determinar el carácter iónico/covalente (parcial) de los enlaces químicos.
Con estas investigaciones, Pauling se convirtió en la máxima autoridad en química estructural de la historia. Su amplio conocimiento lo plasmó en el libro The Nature of the Chemical Bond and the Structure of Molecules and Crystals; publicado por primera vez en 1939, convirtiéndose en uno de los libros científicos clásicos.
A mediados de la década de los años 1930s, Pauling empezó a interesarse en moléculas de interés biológico, especialmente proteínas. Pensaba que la función podría entenderse a partir de su estructura y que ésta podría determinarse por los métodos que él estaba usando para moléculas pequeñas, especialmente métodos de difracción.
Ya en 1934, en conexión con sus investigaciones sobre magnetismo de sustancias químicas, determinó las propiedades magnéticas de la hemoglobina. Ésta es la proteína transportadora de oxígeno en los glóbulos rojos de la sangre en los mamíferos y su estructura y funcionamiento son vitales para entender el mecanismo molecular del transporte de oxígeno y las consecuencias sobre la salud que puede tener su malfuncionamiento.
En 1940 hizo la propuesta novedosa de que la especificidad de las interacciones biológicas se debe a la complementariedad molecular, lo que permite explicar las interacciones entre los antígenos y anticuerpos (con implicaciones en inmunología) y la catálisis enzimática. En esta última área, propone que el aumento de la velocidad de una reacción enzimática se debe a la estabilización del estado de transición por interacción con la enzima. Esta hipótesis explica muchos resultados experimentales y sirve para el diseño de fármacos por inhibición enzimática.
Basándose en la complementariedad molecular, Pauling propuso en 1946 que un gen podría consistir en dos hebras mutuamente complementarias, un concepto que anticipó la propuesta de Watson y Crick para la estructura del DNA.
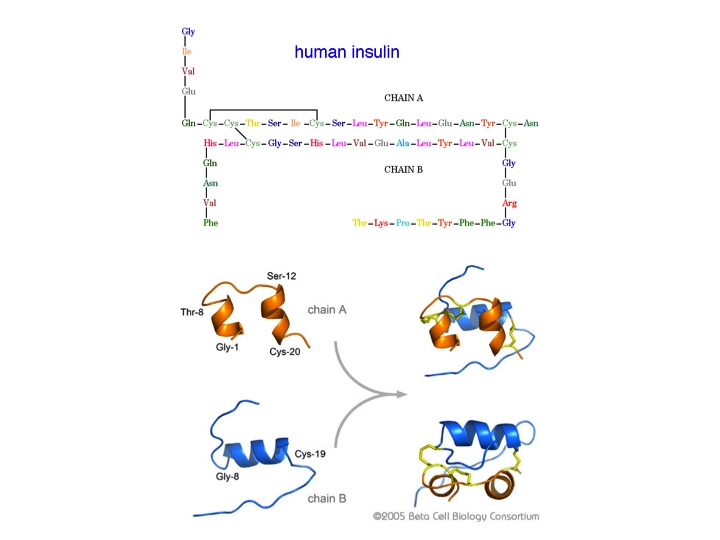
En los años 1940s, Pauling creó el área de la medicina molecular al proponer que la anemia falciforme estaba causada por la mutación de un único aminoácido de los 457 que forman la cadena monomérica de hemoglobina.

En 1948 propuso las estructuras secundarias de las cadenas peptídicas: la hélice alfa y la lámina beta. Su propuesta fue teórica basada en el empleo de modelos moleculares y su profundo conocimiento de la estructura molecular e interacciones no covalente. Poco después se encontró experimentalmente (por difracción de rayos X) que estas propuestas eran motivos estructurales frecuentes en la estructura de péptidos y proteínas.

Con sus propuestas y resultados experimentales sobre la estructura de proteínas, mecanismos de reacciones enzimáticas, complementariedad de proteínas y ácidos nucleicos, y en medicina molecular; se puede considerar a Pauling uno de los fundadores de la biología molecular y su moderna ramificación, la biomedicina.
En la época del Macarthismo en Estados Unidos, estuvo castigado sin pasaporte, lo que le impidió viajar a Inglaterra a para ver las fotografías de la difracción de rayos X tomadas por Rosalind Franklin. Si hubiese visto las fotografías, seguramente hubiese propuesto la estructura de doble hélice del DNA antes que Watson y Crick y la historia de la ciencia hubiese cambiado. Pero esto se ciencia ficción.
Ya en esa época había recibido el Premio Nobel de Química por sus aportaciones a la química estructural, Pacifista convencido y activo (de ahñi los problemas en su país), defendió el desarme nuclear. Por estas acciones, recibió el Premio Nobel de la Paz de 1962 (entregado en 1963). Ha sido la única persona que ha recibido dos Premios Nobel de manera individual: Química (1954) y Paz (1962).
Pauling defendió la hipótesis (que practicó) de que la ingesta de grandes cantidades de vitamina C podrían ser beneficiosa para la salud general. La vitamina C es fundamental en algunas funciones fisiológicas del organismo, como la biosíntesis de colágeno, carnitina y algunos neurotransmisores. La vitamina C es el cofactor de algunas enzimas como la prolinahidroxilasa y la lisina hidroxilasa. La vitamina C también tiene propiedades antioxidantes, siendo un agente eficaz en combatir el estrés oxidativo. Su deficiencia causa el escorbuto.
Como todas las vitaminas, las necesidades diarias son de unos pocos miligramos. Pauling creía que la vitamina C causaba un beneficio general a la salud y abogó por la ingesta maxima de vitamina C, que él mismo practicó tomando hata 100 veces la máxima ingesta diaria de vitamina C. Hoy en día sabemos que el consumo excesivo de vitamina C causa serios problemas de salud, especialmente problemas renales.
Debido a estas prácticas, a veces se ha relacionado a Pauling con la pseudociencia. Sin embargo, Pauling no hizo pseudociencia en su investigación sobre los efectos de la vitamina C. Hizo ciencia, sólo que se equivocó. Plantear hipótesis y teorías que generaciones posteriores prueban erróneas también es ciencia. En la época en la que Pauling empezó a aplicar su teoría (en él mismo), no era descabellado pensar que una vitamina con propiedades antioxidantes podría tener un efecto beneficioso independientemenete de la dosis. También este ejemplo, muestra las dos caras de las sustancias químicas y el hecho de que la dosis determina el efecto.
Sitios de interés y bibliografía:
http://www.nobelprize.org/nobel_prizes/chemistry/laureates/1954/pauling-bio.html#
http://en.wikipedia.org/wiki/Linus_Pauling
Linus Pauling Institute
Linus Pauling in his own words: selected writings, speeches, and interviews
G. R. Desiraju, Nature, 2000, 408, 407.
Libros de Pauling y sobre Pauling
La obra de Pauling en los fondos de la OSU
Pauling y el enlace químico (en los fondos de la OSU)
Pauling y la investigación en hemoglobina y la anemia falciforme (en los fondos de la OSU)
Pauling y la carrera por descubrir la estructura del DNA (en los fondos de la OSU)
The nature of the chemical bond and the structure of molecules and crystals: an introduction to modern structural chemistry
Introduction to quantum mechanics: with applications to chemistry
General Chemistry
Linus Pauling and the Chemistry of Life (escrito por Tom Hager)
Honores recibidos por Linus Pauling (en los fondos de la OSU)
Pauling como maestro
Actividades por la paz (en los fondos de la OSU)
Bernardo Herradón García
CSIC
[email protected]